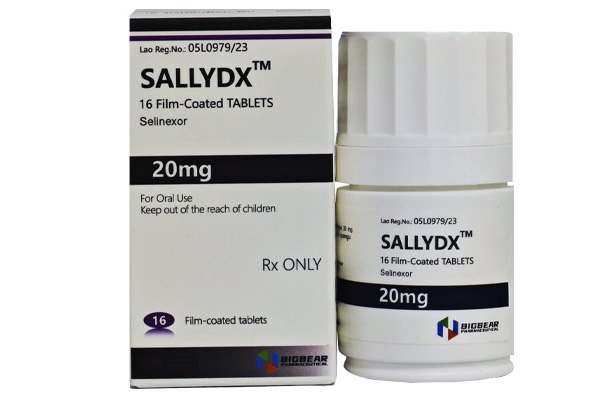
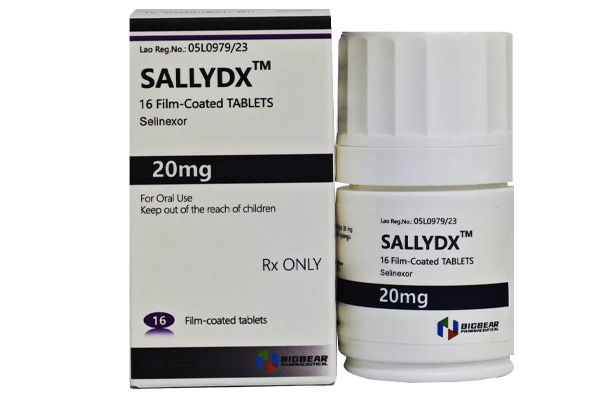
温馨提示: 药品包装不定期更新,请以交付实物为准;为保障用药安全,请严格遵守医嘱或说明书。
塞利尼索 (Selinexor,Sallydx)
全球首个口服XPO1抑制剂,精准阻断核输出,重启肿瘤抑制蛋白。逆转耐药,跨瘤种覆盖。在治疗复发/难治性多发性骨髓瘤等疾病中显示出显著的临床疗效。
所有称呼塞利尼索,Selinexor,希维奥,Xpovio,Sallydx
药品规格
- 20mg*16片/盒
1、请添加医学顾问,确定无误后,再下单。
2、因药品的特殊性,除质量问题外,恕不退换。
3、服药后有不良反应,不属于药品质量问题。
 微信号
微信号 微信号
微信号
 药厂直销
药厂直销 品质保障
品质保障 全球闪送
全球闪送 隐私保护
隐私保护塞利尼索药物新闻
相关栏目
塞利尼索(Selinexor)获第二项肿瘤适应症批准:大B细胞淋巴瘤(DLBCL)
Karyopharm Therapeutics(德琪医药合作伙伴)近日宣布,美国食品药品监督管理局(FDA)已批准塞利尼索(Selinexor)的第二项肿瘤适应症:用于治疗既往接受过至···【更多】
发布时间:2026-04-15文章来源:大熊制药推荐指数:72
塞利尼索(Selinexor)获FDA批准第三个适应症:治疗接受过至少一种既往疗法的多发性骨髓瘤患者
Karyopharm Therapeutics公司近日宣布,美国食品和药物管理局(FDA)已受理其塞利尼索(Selinexor)的补充新药申请(sNDA),寻求批准一个新的适应症,用于···【更多】
发布时间:2026-04-15文章来源:大熊制药推荐指数:70
塞利尼索(Selinexor)——一种治疗多发性骨髓瘤的新型口服药物,即将获得欧盟批准,同时在中国也处于审查阶段!
Karyopharm Therapeutics宣布,欧洲药品管理局(EMA)人用药品委员会(CHMP)已发布积极意见,建议有条件批准塞利尼索(Selinexor)联合地塞米松,用于治疗···【更多】
发布时间:2026-04-15文章来源:大熊制药推荐指数:72
塞利尼索(Selinexor)获欧盟批准,中国国家药品监督管理局受理其上市申请
Karyopharm Therapeutics 公司近日宣布,欧盟委员会已有条件批准塞利尼索(Selinexor)与地塞米松联合用药,用于治疗既往接受过至少四种治疗方案,且其疾病对至少···【更多】
发布时间:2026-04-15文章来源:大熊制药推荐指数:70
欧盟委员会已授予塞利尼索(Nexpovio)联合疗法的全面上市许可
具体而言,欧盟委员会批准塞利尼索联合每周一次硼替佐米(万珂)和低剂量地塞米松(SVd方案),用于治疗既往接受过至少一种疗法的成人多发性骨髓瘤患者。此项决定基于欧洲药品管理局人用药品委员···【更多】
发布时间:2026-04-15文章来源:大熊制药推荐指数:74